 Желатин и мед для суставов
Желатин и мед для суставов
Желатин и его полезные свойства для суставов Желатин – это белковое вещество, которое получают путем денатурации коллагеновых молекул из костей, сухожилий, хрящей и кожи животных. Метод получения желатина изобрел Жан Дарсе, французский химик, еще в восемнадцатом столетии. Следует сразу уточнить,...

Аюрведа при артрите и проблемах с суставами
Что такое Аюрведа Аюрведа – это древняя система знаний, объединяющая в себе разные сферы жизни человека. Зародилась она в Индии несколько тысяч лет назад, само слово означает «знание о долголетии»....
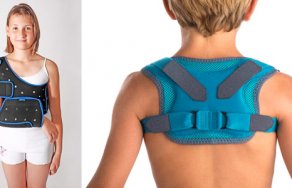
Перелом ключицы лечение и первая помощь
Особенности приспособления Есть два типа приспособлений, которые применяют при травмах ключицы: фиксатор Дезо; косыночный фиксатор. При переломе элемента ключицы наиболее подходящим считают ортез Дезо. Но его используют, лишь если перелом...
Синовит коленного сустава лечение народными средствами
Этапы лечения Первый этап лечебных мероприятий при любом виде синовита основывается на проведении пункции сустава. При помощи специальной медицинской иглы производится эвакуация излишков экссудата для определения его характера в лабораторных...
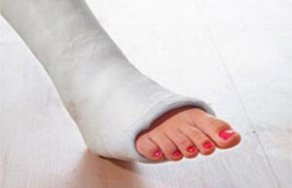
Что делать, если давит гипс
Нога в гипсе полезные советы Ценный совет на форуме дает пользователь-мужчина о питании а. Он считает, основываясь на своем опыте, что в день надо употреблять в обязательном порядке не меньше...

Важные моменты при лечении подагры
Мази, содержащие растительные компоненты Довольно часто применяются мази на растительной основе. Такие мази идеальны для больных с непереносимостью лекарственных химических веществ. Лечение должно быть комплексным и дополняться соблюдением диеты, физиотерапевтическими...
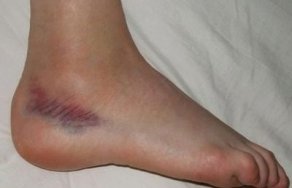
Травмы коленного сустава
Первая помощь Если ребенок упал и закричал, не может подняться или жалуется на боли в руке, в первую очередь нужно спокойно и здраво оценить обстановку: При растяжении связок. Симптомы растяжения...

На сколько дней дают больничный при артрозе коленного сустава
Порядок получения больничного при артрозе первичное обращение при травме При первичном обращении больных к врачу часто выписывается больничный для проведения поддерживающего лечения. Как правило, проблема связана с травмой или инфекционным...
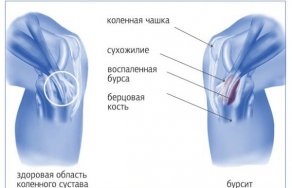
Лфк при бурсите тазобедренного сустава
Подклювовидный тип воспаления восстанавливаем подвижность Подклювовидный бурсит плечевого сустава может появиться на наружной части плечевого сустава. Пострадавшему тяжело отводить руку в сторону. Подклювовидный бурсит нельзя лечить самостоятельно. Самостоятельная терапия усугубить...
Алмаг эпикондилит
Решение есть Совсем недавно в продаже появилось новое уникальное устройство, которое способно избавить человека от многих заболеваний. Это «Алмаг-01» – прибор, действие которого основано на магнитных излучениях. Применение прибора позволяет...
 Желатин и мед для суставов
Желатин и мед для суставов








